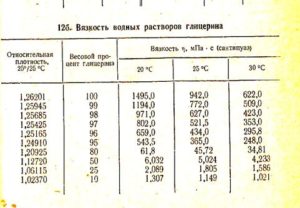
Point de congélation de l'eau
Le processus de congélation a lieu lorsqu'il est refroidi à zéro degré sur l'échelle Celsius. Cela ne s'applique pas à toutes les eaux. Les molécules se fixent sur les impuretés, qui sont des particules de poussière, de sel, etc. Par conséquent, l'eau pure ou distillée, sans la présence de ces mêmes impuretés, sous l'influence des basses températures dans la colonne Celsius, peut rester à l'état liquide plus longtemps que l'eau ordinaire.
Il est également intéressant de noter que si d'autres substances diminuent de volume lors de la congélation, l'eau, au contraire, augmente. En effet, la distance entre les molécules augmente lors de la transition vers l'état solide. Malgré le fait que le volume augmente, la masse n'augmente pas lors de la congélation et pèse autant que l'eau chaude.
Beaucoup de gens se demandent pourquoi l'eau ne gèle pas sous une épaisse couche de glace. Tout physicien répondra que sous une couche de glace, l'eau ne gèle pas, puisque la surface de la glace sert d'isolant thermique.

Pourquoi l'eau chaude gèle-t-elle plus vite que l'eau froide ?
On sait que l'eau chaude ou tiède gèle plus vite que l'eau froide. Incroyable mais vrai. Cette découverte a été faite par Erasto Mpemba. Il a mené des expériences en utilisant la masse congelée et a découvert que si la masse est chaude, elle gèlera plus rapidement. La raison en est, comme l'ont montré des études, le transfert de chaleur élevé de l'eau chaude et chaude.

Le point de congélation de l'eau et l'altitude sont-ils liés ?
Comme vous le savez, la pression change en altitude, de sorte que la température de transition à l'état solide de toutes les solutions aqueuses en altitude diffère de la température sur une surface normale.
Exemples de changements de température en altitude :
- altitude 500 m - le point de congélation de l'eau n'est pas de zéro ° C, comme dans des conditions normales, mais en présence de déjà un ° C;
- hauteur 1500 m - la cristallisation se produit en présence d'environ trois ° C, etc.

Comment la pression affecte le processus de cristallisation de l'eau
Si vous comprenez la relation entre la pression et la cristallisation de l'eau, alors tout est assez simple.
Intéressant! Plus la pression est élevée, plus le taux de transformation de l'eau en cristaux de glace est faible et plus le point d'ébullition est élevé !
C'est tout le secret, et si vous pensez logiquement, alors avec une diminution de la pression, tous les indicateurs vont dans la direction opposée. Par conséquent, il est difficile de cuisiner quelque chose dans les montagnes, car la température à laquelle l'eau bout n'atteint pas cent degrés Celsius. Inversement, la glace fond même à basse température.
Température de cristallisation des solutions aqueuses
L'eau est un bon solvant et se combine donc facilement avec d'autres substances. Les solutions résultantes, bien sûr, gèleront dans des conditions différentes. Envisagez quelques options pour les critères de température pour congeler différentes solutions à base d'eau.
Eau et alcool. Avec une grande quantité d'alcool dans l'eau, le processus de congélation commencera en présence de températures très basses. Par exemple, à un rapport de 60% d'eau pour 40% d'alcool, la cristallisation commencera en présence de moins 22,5 ° C.
Eau et sel. La température à laquelle se produit la congélation est directement liée au degré de salinité de l'eau. Le principe est que plus il y a de sel dans l'eau, plus la température de cristallisation est basse. La façon dont l'eau de mer gèle est directement liée à la teneur en sel.
Eau et soda. La température de cristallisation de la solution est de 44% plus 7°C.
Eau et glycérine, dans un rapport de 80% à 20%, où 80 est la glycérine et 20 est l'eau, la présence de -20 ° C est nécessaire pour geler la solution.
Toutes les valeurs de température fluctuent en fonction du degré de concentration de solutions étrangères ou d'autres substances dans l'eau.
Mesure de la viscosité des liquides avec un viscosimètre Ostwald
Afin de déterminer le coefficient de viscosité ηhis du liquide étudié à l'aide d'un viscosimètre capillaire d'Ostwald (Fig. 6), il faut savoir :
- η0 est la viscosité de l'eau,
- t0 est le temps d'écoulement de l'eau entre les repères a et b,
- tx est le temps d'écoulement du liquide étudié entre les repères a et b,
- ρ0 est la masse volumique de l'eau,
- ρx est la masse volumique du liquide étudié.
Riz. 6. Viscosimètre capillaire d'Ostwald (a, b, d - repères limitant le niveau de liquide, c - capillaire).
La viscosité du liquide étudié est déterminée par la formule (9).
Demande de service
Tâche 1. Déterminer la viscosité de solutions à différentes concentrations.
-
Versez de l'eau dans la branche du viscosimètre qui n'a pas de capillaire (Fig. 6) jusqu'au repère d.
-
Avec une poire, aspirer le liquide à travers le capillaire pour marquer a. Après avoir retiré la poire, boucher le trou du genou gauche du viscosimètre (avec une main, un bouchon, un écouvillon, etc.) (voir Fig. 6). Préparez et allumez le chronomètre en ouvrant le trou du genou gauche et éteignez-le lorsque la marque b coule, déterminant ainsi t0 - le temps d'écoulement de l'eau entre les marques a et b.
-
Répétez les mesures 4 à 5 fois, trouvez le temps moyen.
-
Effectuez les étapes 1 à 3 pour tous les liquides de test.
-
Calculer les coefficients de viscosité des liquides étudiés à l'aide de la formule (9).
-
Entrez les données dans le tableau 1.
Tableau 1
| № | Concentration, % | t1 | t2 | t3 | t4 | t5 | | |
| 1 | ||||||||
| 2 | ||||||||
| 3 | ||||||||
| 4 | ||||||||
| 5 | ||||||||
| 6 |
Tâche 2. Déterminer la concentration d'une solution inconnue.
-
Tracer le rapport de viscosité par rapport à la concentration de la solution
-
Connaissant la viscosité de la solution inconnue, déterminez sa concentration à partir du graphique.
Tableau 2
Densité de l'eau à différentes températures
| ρ, kg/m3 | t, 0C | ρ, kg/m3 | t, 0C |
| 999,13 | 15 | 998,02 | 21 |
| 998,97 | 16 | 997,80 | 22 |
| 998,80 | 17 | 997,57 | 23 |
| 998,43 | 19 | 997,32 | 24 |
| 998,23 | 20 | 997,07 | 25 |
Tableau 3
Viscosité de l'eau à différentes températures
| η, Pa.s | t, 0C | η, Pa.s | t, 0C |
| 0,00114 | 15 | 0,00098 | 21 |
| 0,00111 | 16 | 0,00096 | 22 |
| 0,00108 | 17 | 0,00093 | 23 |
| 0,00103 | 19 | 0,00091 | 24 |
| 0,00100 | 20 | 0,00089 | 25 |
Tableau 4
Densité de solutions de glycérine de différentes concentrations
| AVEC, % | ρ, kg/m3 | AVEC, % | ρ, kg/m3 |
| 5 | 1012,5 | 45 | 1112,5 |
| 10 | 1025,0 | 50 | 1125,0 |
| 15 | 1037,5 | 55 | 1137,5 |
| 20 | 1042,5 | 60 | 1150,0 |
| 25 | 1052,5 | 65 | 1162,5 |
| 30 | 1075,0 | 70 | 1175,0 |
| 35 | 1087,5 | 75 | 1187,5 |
| 40 | 1100,0 | 80 | 1200,0 |
Travail indépendant sur le sujet :
– résolution de situations-problèmes ;
- écoute des résumés
Contrôle final des connaissances :
– résoudre les problèmes de tickets ;
– les réponses aux tickets de contrôle final ;
- résumer.
Devoir pour comprendre le sujet de la leçon
Questions de contrôle sur le sujet de la leçon :
1. Comment appelle-t-on la viscosité d'un liquide ?
2. Quel type d'écoulement de fluide est appelé laminaire ? Turbulent ?
3. Qu'est-ce qui caractérise la formule de Reynolds ?
4. Écrivez la formule de Newton et expliquez la signification physique des quantités qu'elle contient.
5. Quel est le coefficient de viscosité dynamique ? Dans quelles unités est-il mesuré ?
6. Quels fluides sont appelés newtoniens ? Qu'est-ce qui détermine leur coefficient de viscosité ?
7. Quels sont les liquides dits non newtoniens, qu'est-ce qui détermine leur coefficient de viscosité ?
8. Écrivez la formule de Poiseuille, expliquez la signification physique des quantités qui y sont incluses.
9. Quelles méthodes sont utilisées pour déterminer la viscosité d'un liquide ?
10. Parlez des propriétés rhéologiques du sang et d'autres fluides biologiques, de l'utilisation des analyses rhéologiques en médecine.
11. Que montre le gradient de vitesse ? Afficher graphiquement.
12. Quel phénomène s'appelle le frottement interne ?
Tâches de test sur le sujet :
L'APPLICATION DE LA GLYCÉRINE EN CHAUFFAGE EST-ELLE JUSTIFIÉE ?
Des exigences assez élevées sont imposées au liquide de refroidissement pour les systèmes de chauffage. Il doit être résistant au feu et aux explosions, offrir de bonnes performances thermiques et ne pas contenir d'additifs interdits d'utilisation. L'éthylène glycol ou le propylène glycol est utilisé comme base pour la production d'un fluide caloporteur de haute qualité, ce qui garantit également le respect de l'environnement.
Récemment, des liquides de refroidissement antigel à base de glycérine ont fait leur apparition sur le marché. Ce produit est promu principalement par de petites entreprises peu connues sur le marché de l'antigel. La question se pose : glycérine et liquide de refroidissement - leur union est-elle appropriée ?
Et, en effet, les premiers antigels apparus dans notre pays dans les années vingt du siècle dernier étaient fabriqués à base de glycérine. Leurs faiblesses étaient une fluidité insuffisante et une viscosité extrêmement élevée, que les pompes ne pouvaient pas gérer. Ils ont essayé de résoudre le problème à l'aide d'alcool, y compris d'alcool méthylique. Cependant, parallèlement à l'amélioration de la fluidité, de nombreux problèmes sont apparus. Le fait est que le méthanol est un puissant poison psychotrope.De ce fait, le comportement des conducteurs qui reniflaient involontairement un tel antigel défiait parfois toute logique et constituait un danger pour la santé et la vie d'autrui. De plus, l'alcool méthylique a un point d'ébullition bas et lorsqu'il s'évapore, la viscosité du produit augmente immédiatement. Le problème n'a été résolu que lorsque l'éthylène glycol est devenu la base du liquide de refroidissement. Et à la fin des années trente, au début des années quarante, les antigels à l'éthylène glycol ont presque complètement remplacé ceux à la glycérine et au méthanol.
De plus, la glycérine est thermiquement instable, se décompose lors d'un chauffage prolongé, avec la formation d'une substance volatile toxique - l'acroléine, qui a une forte odeur désagréable qui provoque des déchirures. Les produits de décomposition sont toxiques et les précipitations augmentent l'activité corrosive du liquide de refroidissement. En conséquence, les exigences en matière de joints et de pièces en caoutchouc et en plastique non polaires augmentent. En plus d'une viscosité élevée, la glycérine mousse également fortement, ce qui entraîne une aération du système et une mauvaise dissipation de la chaleur.
Les fabricants de liquides de refroidissement à la glycérine tentent de compenser tous les inconvénients ci-dessus en ajoutant divers additifs, notamment des alcools aliphatiques - méthanol, éthanol, propanol. Ces alcools peuvent réduire considérablement la viscosité ou la densité du liquide de refroidissement antigel. Mais ils bouillent déjà à des températures supérieures à 65 degrés, ce qui entraîne une détérioration des performances thermiques du liquide de refroidissement. Ces alcools sont capables de dissoudre le caoutchouc et les polymères, et sont également sujets à la cavitation et à une forte évaporation. De plus, le méthanol est un poison puissant et son utilisation est interdite dans la production de liquides antigel.
Assurer la qualité des liquides de refroidissement à base de glycérine, en particulier avec du méthanol, nécessite l'ajout d'additifs coûteux au mélange. Et bien que le coût de la glycérine soit désormais inférieur au coût des glycols, le package d'additifs pour fabriquer des fluides caloporteurs à base de glycérine de qualité est plus cher que le package d'additifs pour antigel à base d'éthylène glycol et de propylène glycol. Et si le coût de l'antigel à la glycérine sur le marché est inférieur à celui du glycol, cela signifie que le fabricant a simplement économisé sur la qualité et n'a pas ajouté les additifs coûteux nécessaires au produit!
Le choix appartient donc à l'acheteur : soit un liquide de refroidissement fiable et éprouvé à base de glycols, soit une glycérine "cochon dans un poke".
Le choix de notre société, comme la plupart des principaux fabricants d'antigels, est fondamentalement sans ambiguïté - la glycérine ne peut pas être utilisée sous sa forme pure, mais mélangée avec du méthanol, c'est dangereux et criminel !
L'argument principal confirmant notre position sur cette question est que dans toute installation importante et de grande taille, l'utilisation de la glycérine dans les systèmes de chauffage et de refroidissement n'est PAS AUTORISÉE par les normes en vigueur !
GEM
L'éthylène glycol est un produit d'hydratation de l'oxyde d'éthylène en présence d'acide sulfurique ou phosphorique. Fait référence aux alcools polyhydriques. Ne gèle pas à basse température et abaisse le point de congélation de l'eau. Capable d'absorber l'eau de l'air.
Il est vendu en fûts métalliques et plastiques, jusqu'à 227 litres. Ainsi que des cubes en plastique 1000l.
Il est nécessaire de stocker la substance dans un récipient scellé en aluminium ou en acier avec protection anti-corrosion dans un entrepôt fermé sans chauffage. La durée de conservation pour le grade le plus élevé est de 12 mois, pour le premier grade - 3 ans à compter de la date de production.
Nom de l'indicateur Norme
Apparence, odeur Liquide limpide et incolore à texture huileuse. Sans odeur.
Soluble dans l'eau, les alcools, le toluène, le benzène
Densité 1,112 g/cm?.
Point de fusion 12,9 degrés Celsius
Point d'ébullition 197,3 degrés Celsius
Application
En raison de sa capacité à abaisser le point de congélation, le monoéthylène glycol est utilisé dans la production d'antigel et de liquide de frein pour voitures, ainsi que dans la fabrication de cellophane et de polyuréthane. Dans une moindre mesure, il est utilisé dans la production d'encres et d'encres d'imprimerie.
Classe de danger
Désigne les substances combustibles. L'auto-inflammation se produit à une température de 380 degrés, un éclair de vapeur lorsqu'il est chauffé à 120 degrés. Toxique. L'ingestion n'est pas autorisée. Les vapeurs sont moins nocives.
Glycérol
Formule chimique: HOCH2CH(OH)CH2OH
Nom international : Glycérine
N ° CAS: 56-81-5
Qualification: Lutin. "h", GOST 6259-75
Apparence: liquide clair et inodore
Emballage: Bidons de 25 kg, Fûts de 250 kg, 1500 cubes
Conditions de stockage: dans un local sec ventilé à basse température
Synonymes : 1,2,3-trioxypropane
Nous proposons de la Glycérine en bidons, fûts, cubes à des prix compétitifs.
| spécification | |
| Masse moléculaire | 92.10 |
| Substance de base, pas moins de | 99,5 % (réel 99,8 %) |
| Teneur en cendres, pas plus | 0,01 % (en fait moins de 0,1 %) |
| Teneur en eau, pas plus | 0,5 % (en fait 0,1 %) |
| Teneur en chlorures, pas plus | 0,001 % |
| Teneur en sulfate, pas plus | 0,002 % |
| Les métaux lourds, pas plus | 0,0005 % (en fait moins de 0,00005 %) |
| Composés chlorés (comme CL), pas plus | 0,003 % |
| Arsenic, pas plus | 0,00015 % (réel inférieur à 0,00001 %) |
| Couleur (APHA), pas plus | 20 (en fait moins de 10) |
La glycérine est un liquide incolore, hygroscopique, visqueux, inodore et au goût sucré. Miscible dans n'importe quel rapport avec l'eau, l'éthanol, le méthanol, l'acétone, insoluble dans le chloroforme et l'éther. Lorsque le glycérol est mélangé à de l'eau, de la chaleur est libérée et une contraction se produit (réduction de volume). Lorsque le glycérol interagit avec des acides halohydriques ou des halogénures de phosphore, des mono- ou dihalohydrines se forment; avec des acides inorganiques et carboxyliques - esters complets et incomplets, avec déshydratation - acroléine. Le glycérol peut être oxydé, et selon les conditions et la nature de l'agent oxydant, on peut obtenir du glycéraldéhyde, de l'acide glycérique, de l'acide tartronique, de la dihydroxyacétone, de l'acide mésoxalique. La glycérine se trouve dans les graisses et les huiles naturelles sous forme de triglycérides mixtes d'acides carboxyliques.
Application La glycérine est largement utilisée • dans l'industrie pharmaceutique, par exemple pour la production de nitroglycérine, d'onguents médicinaux ; • dans l'industrie alimentaire, par exemple dans la production de liqueurs, de confiserie ; • dans l'industrie cosmétique, dans la fabrication de parfums et de cosmétiques, • dans la production de résines glyptales ; • comme assouplissant pour tissus, cuir, papier ; • comme composant d'émulsifiants, d'antigels, de lubrifiants, de cirages, de savons et d'adhésifs, • comme matière première dans la production de polyalcools, utilisés dans diverses mousses. • comme plastifiant pour cellophane, etc.
À quelle température l'eau gèle-t-elle dans les tuyaux de chauffage d'un immeuble résidentiel
Si la température dans la maison reste à -10 pendant plusieurs jours et qu'il y a de l'eau dans les tuyaux, elle peut geler, ce qui entraînera la rupture des tuyaux. Beaucoup ont probablement vu des batteries de chauffage modernes avec une fonction de vidange d'eau. Presque toutes les batteries modernes sont équipées de la capacité de vidanger l'eau. Ceci est fait pour qu'en cas d'urgence, lorsque la température dans la maison est de -10, l'eau ne gèle pas et ne déchire pas les tuyaux. Si la situation en est arrivée là, nous sympathisons beaucoup avec vous, vous devrez très probablement changer les piles, car lors du gel de l'eau, des microfissures se sont probablement produites qui rendent le fonctionnement ultérieur de ces piles dangereux.
Pourquoi l'eau peut geler dans les tuyaux. Si pendant la saison de chauffage, juste au moment où les batteries se remplissent d'eau, une panne se produit et que l'eau se refroidit, et que la température chute rapidement à l'extérieur, cela peut entraîner le gel des tuyaux.
Nous avons déjà répondu à la question à quelle température l'eau gèle, à titre expérimental, prenez un petit verre, remplissez-le à moitié d'eau et mettez-le au congélateur pendant plusieurs heures, deux heures suffisent pour que l'eau se transforme partiellement en glace.
L'eau est l'une des substances les plus essentielles de notre planète. Il a beaucoup de propriétés qui le rendent, dans une certaine mesure, unique. L'une des propriétés les plus célèbres que même un petit enfant connaît est le gel de l'eau.On sait que 0 degrés Celsius est la température de cristallisation de l'eau. Mais tout n'est pas si simple. Nous examinerons plus loin certaines des subtilités de ce processus.

Densité de la solution de glycérine à 25
La moyenne arithmétique des densités d'alcool et de glycérol.
209.4. 1.047. 25.265.0. 1.060. ... Voir quelle est la densité des solutions aqueuses de glycérine dans d'autres dictionnaires E236 Fichier Formic acid.svg Formule structurelle de l'acide formique L'acide formique méthanoïque est le premier ...
Quelle est la densité de la glycérine à 17 degrés Celsius ?
8
Densité à 25 C, g cm. ... Une solution de glycérine à une concentration de 25% ou plus n'expose pas la contamination microbienne; dans des solutions plus diluées, les micro-organismes s'y multiplient bien.
3,14
Quel liquide a une densité plus élevée, la glycérine ou l'alcool ? Explique
Ssss
TK-April sur le site dans toute la Russie. Concentration, densité et indice de réfraction des solutions de glycérol 15 С. … 1,0594. 1,3633. 25.1.0620.
Calculez la masse molaire des deux substances. Pour l'alcool, elle est moindre (92 g/mol contre 46 g/mol pour l'alcool), et la densité est d'autant plus faible. Quand il s'agit d'alcool éthylique.
Quel est l'intérêt de telles questions ? Les informations sont trouvées dans les moteurs de recherche
La moyenne arithmétique des densités des composants du mélange.
Déterminer quelle masse de glycérol d'une densité de 1,26 g ml doit être prélevée pour préparer une solution aqueuse c.42. ... 111 g d'anhydride phtalique et 46 g de glycérine de densité 28 V sont placés dans un bécher en verre d'une capacité de 0,25 l.
Comment calculer la densité et la viscosité d'un liquide contenant de l'eau, de l'alcool et de la glycérine ?
Pour cela, des rhéomètres sont vendus. vous n'avez rien à compter. juste geler.
triéthylène glycol. propylène glycol. Glycérol. … propylène glycol 40 %. -25 C. ... Densité de solutions aqueuses d'éthylène glycol à différentes températures.
Vous devez connaître le pourcentage de tous les composants du mélange (au moins !)
Certainement pas. C'est-à-dire rechercher les données reçues par quelqu'un.
Aidez-moi, un morceau de glace flottera-t-il dans l'essence, le kérosène, la glycérine ? Pourquoi?
Ce sera dans la glycérine, ça ne flotte pas dans le whisky - la densité est à peu près la même que celle de l'essence
Il augmente également la densité de la solution finie et améliore la qualité des bulles. ... Solution de glycérine bouteille de 25gTula Pharmaceutical Factory LLC. … Solution de tétraborate de sodium en flacon de glycérine 20% 30g, Samara FF, Samara Russie.
La glace est moins dense que le pétrole, donc ce sera le cas.
Comparez la densité de la glace avec la densité de ces liquides. si la densité de la glace est moindre, elle flottera, si elle est supérieure, elle coulera.
Ne sait pas. dépend de quelle pièce. s'il y a suffisamment d'air dans la glace pour la maintenir à la surface, elle flottera, sinon elle ne flottera pas. essayez-le vous-même. le kérosène est bon marché.
Selon la température à laquelle cette glace est refroidie
Le point d'ébullition des solutions aqueuses de glycérine diminue avec une diminution de la concentration de glycérol avec une teneur en eau de 5%, le point d'ébullition est de 160-161, sa densité est de 1,26362 g cm3. … 25 25 C . ZnCl2.
Je n'ai jamais vu de glace flotter dans le réservoir d'essence et la cartouche. Et il l'est certainement))). Il est donc probablement en bas. J'ai vu de la glycérine uniquement dans un flacon et à la chaleur))).
Ooy !
X quantité de glycérol dilué, g A densité de glycérol distillé, g ml ... Les solutions de glycérol à une concentration de 25% et plus ne sont pas sujettes à la contamination microbienne, les solutions plus diluées le sont ...
Un morceau de glace flottera-t-il dans l'essence, le kérosène, la glycérine ?
Découvrez la densité et c'est tout!
Densité des solutions aqueuses d'alcools. Les masses volumiques des solutions aqueuses g cm3 à 20 C sont données pour les substances suivantes : éthanol, 1-propanol, 2-propanol, éthylène glycol, glycérol, D-mannitol.
Oui)))
Si la densité de la glace est inférieure à la densité du liquide, alors la glace flottera
Quelle est la densité de la glycérine à une température de 24 gr. AVEC?
Glycérine Degrés Celsius020406080100120140169180Densité g/cm3126712591250123812241208118811631126
Pour une température de 24 degrés = déterminer par interpolation entre 20 et 40 degrés
Calculer le point d'ébullition d'une solution à 8 % de glycérol C3H6O3 dans l'acétone. La réponse est 57,7oC. 4.Une solution dont 100 ml contiennent 2,3 g ... Prendre la densité de la solution égale à un. Réponse 608 Pa. Ticket 14 25 1. Combien de grammes de BaCl2 2H2O ...
Questions sur la chimie))) et la physique. Quel liquide est plus dense que l'eau et conduit également l'électricité mais pas le métal ?
Glycérine, éthylène glycols, formamides, butyrolactone, presque tous les acides, amines. et beaucoup plus.
Concentration d'acide sulfurique, % en masse. Densité à 25 C, g cm.... 25,60-0,1950 0,000 8 - humidité relative,% - indice de réfraction d'une solution aqueuse de glycérol à 25 C pour la ligne D sodium - température de la solution, C ...